Freiburger Forscherteam um ehemaligen FRIAS-Fellow Stefan Schiller veröffentlicht richtungsweisende Forschungsergebnisse in zwei Nature Zeitschriften
Beide Publikationen beschäftigen sich mit Verfahren, die das Funktionsspektrum von Zellen erweitern und somit letztlich die Herstellung von Basisrohstoffen für die chemische Industrie ermöglichen könnten, welche für eine nachhaltige Bioökonomie grundlegend sind.
Die Gruppe um Stefan Schiller nutzt maßgeschneiderte Proteine als Bausteine, um aus ihnen Nanosysteme mit neuen physikalischen, chemischen und biologischen Eigenschaften aufzubauen. Die nachhaltige und ressourcenschonende Herstellung dieser Proteine erfolgt beispielsweise im natürlichen Energie- und Stoffkreislauf von Zellen. Zu diesem Zweck forscht der Arbeitskreis daran, beispielsweise Bakterien mit zusätzlichen Elementen auszustatten – etwa mit Enzymen, Transportern, Schaltern und Organellen, den Organen der Zelle.
So konnten die Forscher, gemeinsam mit Kollegen der Universität Konstanz, im März 2015 die Ergebnisse ihrer Studie zur Protein-Adaptor-basierten-Nano-Objekt-Anordnung (PABNOA) in einer Publikation im Journal Nature Communications veröffentlichen. PABNOA erlaubt es, mithilfe von ringförmigen Proteinen Goldnanopartikel zu verschiedenen Strukturen anzuordnen, wobei der Abstand zwischen diesen Partikeln exakt definiert ist (siehe Abb. 1). Dadurch lassen sich biobasierte Materialien mit neuen optischen und plasmonischen Eigenschaften herstellen. Die Nanoplasmonik beschäftigt sich mit kleinsten elektromagnetischen Wellen, die von Metallpartikeln ausgehen, wenn diese mit Licht interagieren. Nach dem gleichen Prinzip wie diese Materialien könnten auch Nanosysteme, die Licht in elektrische Energie umwandeln, sowie biobasierte Materialien mit neuen magnetischen Eigenschaften entwickelt werden.
|
Abb. 2 |
Organellen standen im Zentrum weiterer Studien des Teams um Stefan Schiller. In ihrem im Januar 2015 veröffentlichten Artikel in Nature Materials konnten die Forscher zusammen mit weiteren Gruppen aus Freiburg und Ungarn ein lange vorherrschendes Paradigma in der Biologie widerlegen: sie zeigten, dass Organellen – die Organe der Zellen – um weitere Funkionen erweitert werden können und sogar mithilfe genetischer Baupläne gänzlich neu gebildet werden können. |
|---|
Während weniger komplexe Zellen, z.B. Bakterienzellen, kaum Organellen aufweisen, besitzen höhere Zellen, also Pflanzen- und Säugerzellen, mehrere unterschiedliche Organellen wie beispielsweise den Zellkern, die Mitochondrien, Lysosomen und andere mehr.Wie Organe im menschlichen Körper erfüllen diese Organellen verschiedene Funktionen wie den Abbau von Stoffen oder die Energiebereitstellung.
Dem Team um Stefan Schiller gelang es nun zu zeigen, dass diese Organellen neu konstituiert und funktionalisiert werden können. Bisher herrschte die Annahme vor, dass Organelle nur aus schon bestehenden Organellen konstituiert werden können. Da Zellkompartimente höherer Zellen wesentlich aus Lipiden konstituiert werden, die aber als sekundäre Genprodukte nicht direkt unter genetischer Kontrolle steuerbar sind, entwickelten die Forscher einen neuen Ansatz, der auf der Verwendung amphiphiler, d.h. sowohl hydrophiler als auch lipophiler, Proteine anstatt von Lipiden beruht. Diese Proteine besitzen wie Lipide einen wasserfreundlichen und einen wasserabstoßenden Molekülteil. Diese Eigenschaft erlaubt es den amphiphilen Proteinen, sich selbständig im wässrigen Innenraum der Zelle zu organellähnlichen Kompartimenten zusammenzulagern. Diese Organellen können nun für erweiterte biotechnologische Anwendungen studiert werden und bilden somit die Grundlage für neue Ansätze bei der Erforschung biomedizinischer Prozesse und Anwendungen in der Biotechnologie, der Chemie und Pharmazie. Insbesondere für die chemische Industrie könnten durch die funktionelle Erweiterung von Bakterienzellen wichtige Ausgangsstoffe produziert werden, für deren Biosynthese es bisher keine Strategien und Verfahren gab.
Für die Realisierung dieser Ideen hat Schiller 2014 den mit ca. 3,4 Mio Euro dotierten Forschungspreis „Nächste Generation biotechnologischer Verfahren – Biotechnologie 2020+“ des Bundesministeriums für Bildung und Forschung erhalten.
Abb. 1: Die schematischen Modelle und elektronenmikroskopischen Aufnahmen zeigen definierte Architekturen aus Proteinen (im Modell grün) und Goldnanopartikeln.
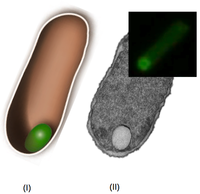
Abb. 2: Schema, elektronenmikroskopische Aufnahme und Fluoreszenzbild von Organellen
Weitere Informationen erhalten Sie unter: http://www.pr.uni-freiburg.de/pm/2015/pm.2015-04-16.58
Originalpublikation:
- Organellen: Matthias C. Huber, Andreas Schreiber, Philipp von Olshausen, Balázs R. Varga, Oliver Kretz, Barbara Joch, Sabine Barnert, Rolf Schubert, Stefan Eimer, Péter Kele & Stefan M. Schiller: Designer amphiphilic proteins as building blocks for the intracellular formation of organelle-like compartments. Nature Materials 14, 125–132 (2015). doi:10.1038/nmat4118
- Proteinbaupläne und Nanotechnology: Andreas Schreiber, Matthias C. Huber, Helmut Cölfen & Stefan M. Schiller: Molecular protein adaptor with genetically encoded interaction sites guiding the hierarchical assembly of plasmonically active nanoparticle architectures. Nature Communications 6, Article number: 6705 (2015). doi:10.1038/ncomms7705 www.nature.com/ncomms/2015/150327/ncomms7705/metrics
04/2015